2017年狂犬疫苗批签发及市场需求情况
2018/3/9 14:30:46 三胜产业研究中心 https://www.china1baogao.com/
| 本文相关报告 REPORTS | |
 | 2017-2022年中国狂犬疫苗行业运行指标监测与投资前景预测咨询报告 |
| 制造业是国民经济的主体,是科技创新的主战场,是立国之本、兴国之器、强国之基。当前,全球制造业发展格局和我国经济发展环境发生重大变化,必须紧紧抓住当前难得的战略机遇,突出创新驱动,优化政策环境,发挥制度... | |
狂犬病是一种人畜共患急性传染病,病死率达100%,全球每年因狂犬病发作死亡人数约为5.5万人,绝大多数死亡发生在亚洲和非洲的农村地区,接种狂犬疫苗是预防该病的最有效手段。全球每年至少有1500万人接受暴露后预防,其中大多数人生活在中国和印度。目前我国常用的狂犬疫苗依据细胞基质种属差异可分为两大类:1、动物细胞狂犬疫苗:非洲绿猴肾(VERO)细胞、地鼠肾细胞、鸡胚;2、人二倍体细胞疫苗(HDCV, human diploid cell vaccine):人源细胞(健康的人胚肺成纤维细胞)MRC-5、WI-38。地鼠肾细胞:1960s 发展起来的技术,效价低、免疫效果不好,逐步被淘汰。鸡胚细胞:诺华采用,1965 年发展起来的技术。Vero 细胞:辽宁成大、长春长生等采用,1980s 年发展起来技术,表达量高,效价高,稳定性好,副作用小,价格低,较高性价比的主流产品。人二倍体:狂犬疫苗的金标准,相较于动物源性细胞狂犬疫苗的局部和全身不良反应发生率更小,理论上无致肿瘤风险,在国外已经有 30 多年的临床使用经验,但其产量较低、价格昂贵,适用于孕妇和儿童。《中国药典 2005 年版》规定冻干人用狂犬病疫苗(Vero 细胞)DNA 残留量标准为“不高于 100pg/剂”,但当时国内上市的所有 Vero 细胞狂犬疫苗生产企业都达不到该标准,国家也没有统一的 DNA 残留量检测标准品,所以国家药监局及中检院进行批签发时并没有对狂犬疫苗 DNA 残留量要求检验。2009 年 4 月 2 日,中检院发布《关于人用狂犬病疫苗(Vero)细胞批签发检验增加项目的通知》(中检生[2009] 609 号),要求“将对此后申请批签发的人用狂犬病疫苗(Vero 细胞)在成品疫苗中实施 DNA 残留量检测,达不到规程标准要求的将不予签发”。随后又下发了《关于进一步规范生物制品质量控制要求的通告》(2009 年第 6 号),要求“病毒性疫苗生产中仅允许在细胞制备、细胞增殖过程中使用抗生素”,“注射用冻干制剂中不得添加任何防腐剂”。由于赛诺菲的狂犬疫苗(Vero 细胞)工艺中 DNA 残留量达不到国内标准,随即在国内退市。国内也有多家企业 2011 年后停止批签发。2017 年三季度,狂犬疫苗批签发 5539.6 万瓶,同比增 29.4%。狂犬疫苗前 4 家成大生物、长春长生、广州诺诚、宁波荣安已形成垄断格局。中标价:Vero 细胞的中标价约为 45~60 元/瓶,人二倍体价格为 280 元/瓶(1 人次接种5 瓶)。人二倍体价格约为 vero 细胞系的 5 倍。预计国内狂犬疫苗市场约30亿元。
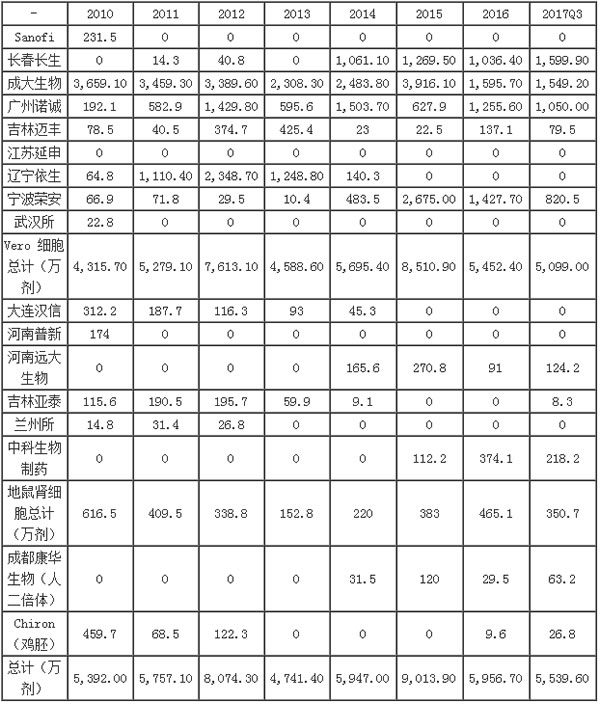
2010~2017Q3 年狂犬疫苗批签发情况
免责声明:
1、本站部分文章为转载,其目的在于传递更多信息,我们不对其准确性、完整性、及时性、有效性和适用性等作任何的陈述和保证。本文仅代表作者本人观点,并不代表本网赞同其观点和对其真实性负责。
2、中国产业信息研究网一贯高度重视知识产权保护并遵守中国各项知识产权法律。如涉及文章内容、图片等版权问题,烦请联系QQ:307333508,或在线反馈、link@china1baogao.com、0755-22213881,我们将及时沟通与处理。